الجزء في المليون (ppm) هو تعبير يستخدم في الفيزياء والكيمياء للنسب الصغيرة جدا من تركيز مادة A في المادة B, اي ان تركيز A يساوي واحد من مليون جزء من المادة B.
فمثلا 1 ppm ثاني اكسيد الكربون يساوي (0,000001) من اجمالي حجم المادة التي ضمن تركيبتها ثاني اكسيد الكربون.
ومثلا في الغازات المثالية فان الحجم المولي هو نفسه بغض النظر عن نوع الغاز المعني, حيث يمكن حساب الحجم المولي باستخدام قانون الغاز العام:
حيث ان:
p= الضغط بـ Pa
VM= الحجم المولي, ميللغرام لكل متر مكعب
M= الكتلة المولية
R= ثابت الغاز
T= درجة الحرارة بكلفن
فلو كانت الحرارة عند 20 درجة مئوية والضغط هو الضغط الجوي (101300 Pa) فانه ببعض التحويل نحصل على الحجم المولي والذي يساوي 24,06 متر مكعب لكل كيلومول ( ثابت الغاز يساوي 8314).
واذا كانت قيمة الكتلة المولية معلومة لدينا فحينها يمكننا حساب التركيز والتحويل من ppm الى mg/m3:
فلو افترضنا ان تركيز ثاني اكسيد الكربون هو 1000 ppm في حرارة بدرجة 20 مئوية ( 295.15 كلفن ) وعند الضغط الجوي, فان تركيز ثاني اكسيد الكربون يساوي:
ارجو ان تكونوا قد استفدتم من الموضوع




 التحويل ما بين وحدة الميللي غرام للمتر المكعب ( mg/m3) ووحدة الجزء في المليون (ppm)
التحويل ما بين وحدة الميللي غرام للمتر المكعب ( mg/m3) ووحدة الجزء في المليون (ppm)
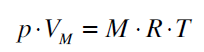
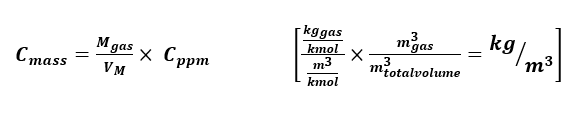
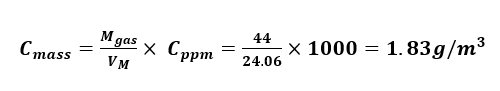
 رد مع اقتباس
رد مع اقتباس