الخيطيات (داء -)
الخيطيات filaria هي مجموعة من الديدان الممسودة (مدورة) nematode يتطفل بعضها على الإنسان فيسبب له مرضاً. تتوضع الكهلة منها تبعاً لنوعها في اللمف أو الجلد، كما تطلق بعد تزاوجها، في جسمه، خييطيات أو يرقاتmicrofilaires تشاهد في جلده أو دمه.
يكثر انتشار هذه الطفيليات في المناطق المدارية وتحت المدارية، ولا تحدث الإصابة بها مباشرة بل تكون دوماً بوساطة ثوي ناقل.
أنواع داء الخيطيات
1- داء الخيطيات اللمفي: ويشمل الأمراض التي تنجم عن الإصابة بالفخرية البنكروفتية Wuchereria bancrofti، والبروجية الملاوية Brugia malayi، والبروجية التيمورية Brugia timori.
أ ـ داء الخيطيات بالفخرية البنكروفتية أو داء الفخريات Wuchereriasis: تتوطن هذه في معظم أقاليم العالم الدافئة والرطبة وتشيع في المناطق ذات الإصحاح السيئ الذي يساعد على توالد البعوض. وتشمل الإصابة بها بؤراً في أمريكا اللاتينية وإفريقيا وآسيا وجزر المحيط الهادئ. والبعوض الناقل لها هي أنواع من الباعضة Culex والإنفيل Anophele والزواعج Aedes. تنتقل اليرقات إلى الإنسان بعد لدغة البعوضة المصابة فتدخل الأوعية اللمفية الناحيّة ويكتمل نموها فيها. وتعيش الكهول في الأوعية الدموية والعقد اللمفية. تلد الإناث يرقات (خييطيات) لا تظهر في الدم إلا بعد زمن حضانة يمتد من 6 إلى 12 شهراً فتحدث شكلين من المرض. تشاهد في أحدهما اليرقات في الدم المحيطي في أثناء الليل، في حين تشاهد اليرقات في الشكل الآخر باستمرار فيه.
إصابة ضخمة بداء الفيل في الساق والصفن
تشمل المظاهر السريرية، في الأقاليم التي يتوطن فيها الخمج، أناساً دون أعراض، وآخرين بأعراض تضم حمى حادة وراجعة مع التهاب العقد والأوعية اللمفية، وأناساً بعلامات مزمنة تشمل قيلة مائية (أدرة)، وبيلة كيلوسية، وتؤدي الوذمة المزمنة الضخمة إلى داء الفيل في الأطراف وأعضاء التناسل والثدي. كما تتظاهر بعض الإصابات بربو انتيابي ليلي ومرض رئوي خلالي مزمن.
ب ـ داء الخيطيات الملاوية: وتسببه البرجية الملاوية، وأكثر ما تصيب الجماعات التي تعيش في مناطق زراعة الأرز في جنوبي الهند وسريلانكا، وسواحل الصين الشمالية والمتوسطة، وكورية الجنوبية.
تشبه أعراضها أعراض الخيطيات البنكروفتية وقد تسبب تفاعلاً التهابياً أرجياً في زمن لا يزيد على الشهر من بدء الإصابة، لكن اليرقات (الخييطيات) لا تظهر إلا بعد 2 إلى 3 أشهر.
ج ـ داء الخيطيات التيمورية: وتسببه البروجية التيمورية، ويشاهد في الجزر الشرقية لإندونيسية ولا تختلف أعراضها عن أعراض البروجية الملاوية.
يتم الشك بإصابة الخيطيات اللمفاوية استناداً إلى العوامل الوبائية، والأعراض السريرية، وأمام مريض يظهر ارتفاعاً كبيراً في الحمضات تزداد كثرة في كل هجمة لمفاوية، وإلى إيجابية التفاعلات المصلية كالومضان المناعي immunofluorescenceوالرحلان الكهربائي electrophorese، لكنه لا يؤكد إلا برؤية الخييطيات في محضر مهيأ من الدم المحيطي (وخزة إصبع)، أو في الدم المنحل في حجيرة التعداد.
تختفي الخييطيات بسرعة من الدم بإعطاء ثنائي الإيتل كاربامازين diethylcarbamazine والإيفرمكتين ivermectin ولكنهما قد لا يؤثران في الطفيليات التامة النمو لذا يجب إعادة العلاج سنوياً.
2- داء اللويات loase: وعاملها الخامج اللوا اللوية Loa loa تشاهد الإصابات بها بكثرة في وسط إفريقيا المدارية وغربها، وفي جنوب حوض نهر الكونغو. تنتقل إلى الإنسان بلدغ ذبابة الخيل أو ذبابة الغزال من جنس ذهبية العيون chrysops، التي ابتلعت الدم المحتوي على اليرقات. ولا تظهر أعراض الخمج عادة إلا بعد عدة سنوات، ولكن قد تحدث مبكرة بعد أربعة أشهر. تتصف الإصابة بها بهجرة الدودة البالغة من خلال نسج تحت الجلد وربما النسج الأعمق، فتسبب ورماً بحجم عدة سنتمترات في أي جزء من الجسم البشري (تورمات كالابار). وقد يسبق الورم ألم موضعي، ولاسيما في اليدين والكاحلين، تصاحبه حكة. وربما أحدثت الإصابة تفاعلات أرجية وشروية وحمى. ويمكن لهذه الخيطية أن تجتاز العين وتظهر تحت الملتحمة، كما أنها قد تسبب مضاعفات عصبية ونفسية وكلوية ومفصلية وشغافية.
ومما يوحي بالإصابة بها الوذمات والعلامات العينية وزيادة الحمضات الثابتة، وإيجابية الفحوص المناعية كالومضان المناعي. ويؤكد التشخيص بكشف اليرقات في الدم المحيطي في أثناء النهار في ساعات الظهيرة، والتي ربما ظهرت بعد 5 إلى 6 أشهر من حدوث الخمج. قد تبقى هذه الخيطيات في جسم الإنسان أحياناً سنوات طويلة تصل إلى 17 عاماً.
تكون المعالجة بثنائي إيتيل كاربامازين الذي يقضي على الخييطيات وقد يقتل الديدان البالغة فيحدث الشفاء، كما أن الإيفرمكتين يخفض حمل الدم من اليرقات (الخييطيات). وإعطاء البندازول albendazole يخفض حمل اليرقات ببطء وقد يقتل هو أيضاً الديدان البالغة. ويوصى بإزالة الدودة البالغة المهاجرة لتحت ملتحمة العين جراحياً إن أمكن.
3- داء كلابية الذنب onchocercose: أو العمى النهري: وتشاهد الإصابات بها في اليمن وفي إفريقية في منطقة تمتد من السنغال إلى إثيوبية وأنغولا وملاوي، وفي بعض مناطق غربي إفريقيا؛ كما تشاهد في أمريكا الجنوبية في المكسيك وفنزويلا وغواتيمالا وكولومبيا والإكوادور وبعض مناطق البرازيل.
ينتقل الخمج إلى الإنسان بلدغة أنثى الذباب الأسود من جنس الذلفاء simulie حينما تكون مصابة، فتسبب له مرضاً مزمناً غير مميت يترافق بعقيدات ليفية في نسج تحت الجلد، ولاسيما في الرأس، والمنكبين والحزام والأطراف السفلية. يشاهد الطفيلي البالغ في العقيدات وبجانب سمحاق العظم وقرب المفاصل. تلد الأنثى يرقات تهاجر خلال الجلد محدثة طفحاً وحكة شديدة، وتغيراً في انصباغ الجلد وضموراً فيه ووذمة. وقد يؤدي فقدان مرونة الجلد إلى الأربية المتدلية. وكثيراً ما تصل اليرقات إلى العين فتسبب اضطرابات إبصارية وعمى. ويقدر عدد المصابين بأعينهم في عام 2000 بنحو 25 مليون إنسان منهم 5 ملايين فقدوا بصرهم.
ومما يدفع للشك بالإصابة بهذه الخيطية الحكة والعقد وكثرة الحمضات والتفاعلات المناعية؛ ولا يتم تأكيد التشخيص إلا بأخذ خزعة جلدية سطحية، وإظهار اليرقات (الخييطيات) في محضرات بالفحص المجهري، أو باستئصال العقيدات والعثور فيها على الديدان البالغة. ويؤكد تشخيص إصابات الحالات العينية برؤية اليرقات بالمصباح الشقّي slit-lamps في القرنية أو في البيت الأمامي، أو في الجسم الزجاجي.
يعطى الإيفرمكتين ivermectin وحده أو مع السورامين للمعالجة، وهو نوعي لهذا الطفيلي فيؤثر في اليرقات وفي الديدان الكهلة في الجلد والعين خلال مدة تمتد من 6 إلى 12 شهراً. كما أن سيترات ثنائي إيتيل كاربامازين فعال ضد اليرقات.
4- داء التنينات Dracunculose: وتسببه التنينة المدينية. تشاهد أخماج هذا الطفيلي في اليمن وشبه الجزيرة العربية والعراق، كما تشاهد في إيران وتركستان وباكستان والهند ولاسيما في الأقاليم الجافة. وهناك إصابات بها في إفريقيا الاستوائية والغربية والمتوسطة وحوض النيل. ويختلف الانتشار المحلي للخمج اختلافاً كبيراً، ففي بعض الأماكن يكون معظم السكان مصابين في حين لا تشاهد في مناطق ثانية إلا عند قلة نادرة.
إصابة في منطقة مفصل الركبة بداء التنينات وترى الدودة الكهلة
يصاب الإنسان بها بابتلاع نوع من البلعط cyclops المخموج بها، عندما يشرب ماءً من آبار مفتوحة أو برك ملوثة. تتحرر اليرقات في المعدةأو العفج، ثم تهاجر خلال الأحشاء لتصير ديداناً بالغة، تهاجر أنثاها بعد التزاوج إلى نسيج تحت الجلد وغالباً في الساقين. يظهر عادة على أحد الطرفين السفليين، ولاسيما في منطقة القدم حويصل صغير عندما تكون الأنثى مستعدة لإخراج يرقاتها. وقد يسبق تكون الحويصل ألم حارق وحكة في الجلد، في منطقة الآفة، مع حمى وغثيان وقياء وإسهال وضيق نفس وشرى وكثرة الحمضات. تطرح الدودة اليرقات، بعد أن ينفجر الحويصل، كلما جرى غمر الجزء المخموج بالماء. إن إنذار الإصابة حسن ما لم توجد ديدان عدة، أو ما لم يحدث خمج جرثومي يسبب عقابيل.
يتم التشخيص باكتشاف شريط صلب تحت الجلد يمثل الدودة البالغة أو برؤية اليرقات تحت المجهر التي يمكن استخراجها بوضع ماء على نهاية الخيطية، أو بإحداث منطقة باردة حول الجرح بكلورور الإيتيل.
إن استخراج الدودة بلفها حول قضيب في زمن يمتد عدة أسابيع هي طريقة مجدية. وقد استعمل الليبندازول والمترونيدازول والمبتدازول لتخفيف الالتهاب وسرعة طرد الدودة.
عدنان تكريتي
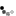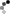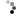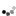







 رد مع اقتباس
رد مع اقتباس








